摘 要:以球形镁铝合金(Al12Mg17)颗粒为原料,在空气中直接燃烧合成氮化铝(AlN)晶体。实验样品堆积在直径为1 cm的区域内,使用乙烷火焰点燃。使用高速摄像仪记录燃烧合成过程。借助XRD和SEM对原料和产物的组成及结构进行分析,并使用TG-DSC分析合金的热力学性质。结果表明:镁铝合金中的铝可以全部转化为AlN晶体。合金的点火温度约为 494.4 ℃,一旦点燃,不需要外界热源的持续加热,样品可持续燃烧。燃烧开始后,合金颗粒中镁快速汽化,与空气中氧发生优先反应,并耗掉颗粒周围的氧气,使氮气进入液态铝表层,生成氮化铝。燃烧产物有明显分层,检测结果表明上层产物为白色氧化镁,下层产物为黑色氮化铝晶体。合成过程中,镁对氮化铝的形成起着积极的促进作用。
关 键 词:AlN;镁铝合金;燃烧
氮化铝具有优良的性能,被广泛应用在半导体,陶瓷以及光电等领域[1-3]。传统合成氮化铝的方法主要包括碳热还原法、直接氮化法和自蔓延高温合成法等[4]。对于直接氮化法和自蔓延高温合成法,由于氮气渗透能垒的存在,反应往往需要在高压下进行。并且,反应对氮化温度有着严格的要求[5-7]。对于碳热还原法[8],虽然能获得较为纯净的氮化铝,但是其还原温度一般在 1000 ℃以上,并且由于在合成过程中使用了过量的碳粉,碳热还原法制得的氮化铝还需进行脱碳处理,合成耗时且工艺复杂,对设备要求较高。近几年的研究发现,当纳米铝粉在空气中燃烧时,产物中会含有大量的氮化铝。因此,将纳米铝粉在空气中直接燃烧生成氮化铝为人们合成氮化铝提供了一种新的思路与方法[9-10]。相对于其它合成方法,纳米铝粉在空气中直接燃烧合成AlN具有反应速度快,反应温度低且可以在常压下进行等特点。一经点燃,燃烧产生的热量足以维持燃烧,不需要额外的热源加热。但是该方法点火温度高,产率较低且反应过程中会产生氧化铝杂质等缺点又限制了其进一步发展。
本研究提供合成氮化铝的一种新方法,即采用质量比为1 :1的镁铝合金代替单质铝在空气中直接点燃合成氮化铝,对其燃烧过程和燃烧产物进行分析。并对氮化铝的形成机理进行了讨论。
1 实验方法
实验所用的镁铝合金粉由唐山威豪镁粉有限公司提供。镁粉(99.9%)与铝粉(99.9%)在液体熔融状态下、氩气环境中按质量比为1 :1进行混合,然后雾化成型得到均匀的球形粒子。表1列出实验使用的主要仪器设备及其生产厂家,其中 TG-DSC测试在空气中进行,空气流速40 mL/min,升温速率10 ℃/min,测试温度范围为室温到1000 ℃。用高速摄像仪记录合金在空气中的燃烧过程,使用丁烷火焰点燃合金,其火焰温度可达1300 ℃。合金被点燃后,移开外部加热源,使合金自发燃烧得到燃烧产物。
2 结果与讨论
如图1所示,镁铝合金主要由镁铝中间体Al12Mg17相组成,没有检测到单质镁和单质铝。粒子为均匀的球体,部分粒子出现团聚现象。粒子表面光滑,可以观察到少量纳米级的氧化物颗粒。样品粒度分布均匀,中位径约为108 μm。
如图2所示,在468.5 ℃左右,镁铝合金的DSC曲线上出现一个明显的吸热峰,这与镁铝合金中间体Al12Mg17相的熔化峰相对应[11]。Shih等[12]研究发现,在加热过程中Al12Mg17会发生熔化并分解,生成单质镁和单质铝,其分解过程如下:
分解产生的镁随即与氧气发生反应,生成氧化镁,因此在 DSC曲线上观察到一个强的放热峰(494.4 ℃)。此时铝不发生反应,而是以单质形式存在于样品中[13]。在 657.8 ℃附近观察到一个较小的吸热峰,对应铝的熔化,说明当 Al12Mg17熔化且发生分解后,所生成的铝单质处于固态。
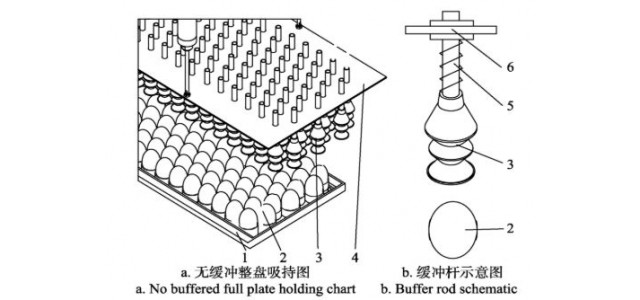
如图3所示,AIN的合成可以大致分为三个阶段。第一阶段为点火阶段,样品发生局部燃烧并逐渐扩散到整个样品堆,此时可以观察到部分粒子飞散到空中并发生微爆的现象。第二阶段为气相燃烧阶段,粒子不再从样品中飞出,样品表面形成稳定的、散发出明亮白光的火焰。在火焰顶部可以观察到白色烟雾。根据上面的分析可知,在加热过程中,镁首先发生燃烧且燃烧主要集中在气相,因此此时所形成的气相火焰应是气态镁的燃烧火焰。当气相反应结束之后,反应进入第三阶段,即液相反应阶段。从图3中可以看出,气体火焰消失,没有观察到明显的白光,反应在气相阶段产生的氧化物壳下继续进行。
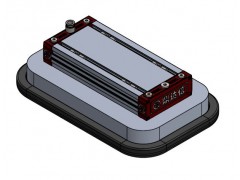
样品在空气中的燃烧产物分为两层:上层为白色多孔状物质,下层为黑色熔融物(如图4所示)。使用 XRD分别对两层物质进行检测,结果如图5所示。上层白色物质为MgO,下层黑色熔融物为AlN。在上层氧化物中只检测到 MgO,而没有检测到Al2O3或AlN,进一步说明在燃烧的第二阶段,观察到的气相火焰是由气态镁燃烧产生的。镁燃烧生成的凝固性产物 MgO一旦出现立即发生凝结,形成白色烟雾。固态的MgO颗粒沉降到粒子表面形成MgO产物层。使用SEM对AlN层进行观察(图6)。AlN颗粒为空心壳体且发生团聚现象,说明在燃烧过程中,粒子虽然保留了原有的形状,但铝发生了熔化,熔融的铝充斥在粒子之间,起着粘结剂的作用。这也解释了为什么在反应的第一阶段观察到了粒子的飞散而在气相反应阶段没有观察到相同的现象。壳体内部均可以看到形状不规则的小孔。壳体的内表面较为光滑,外表面则能观察到明显的AlN晶须。
表1 实验使用的主要仪器设备及其生产厂家
Table 1 Main instruments used in the test and their manufactures

Gromov等[9]研究表明,纳米铝单质在空气中燃烧时,铝被空气中的氧气氧化成 Al2O3,生成的 Al2O3和未反应的铝单质反应生成 Al2O,当温度升高,空气中的N2会将Al2O中的氧置换出来,其反应过程如下:

图1 镁铝合金性质分析
Fig.1 Analysis of the Mg-Al alloy powder
(a)XRD pattern;(b)Size distribution;(c)SEM image;(d)Magnified area in(c)
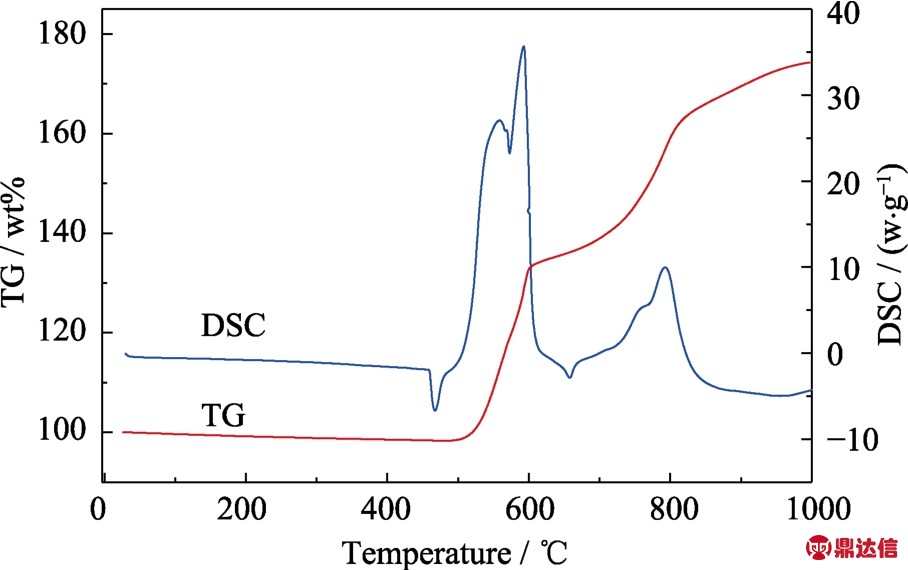
图2 镁铝合金在空气环境下的TG-DSC曲线
Fig.2 TG-DSC curves for Mg-Al alloy heated in air

图3 使用高速摄像仪记录的镁铝合金粒子在空气中的燃烧过程。
Fig.3 Combustion process of Mg-Al alloy in air recorded by a high-speed camera

图4 镁铝合金在空气中的燃烧产物
Fig.4 Combustion products of Mg-Al alloy particles burned in air
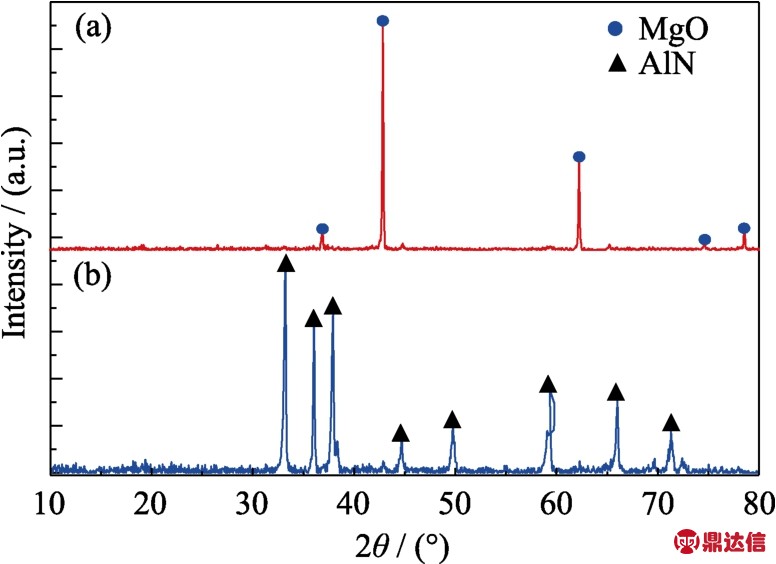
图5 镁铝合金在空气中的燃烧产物的XRD图谱
Fig.5 XRD patterns of the combustion products of the Mg-Al alloy particles in air
(a)Upper white oxide;(b)Lower black material

图6 镁铝合金在空气中燃烧产生的AlN颗粒(a)和AlN晶须(b)的SEM照片
Fig.6 SEM images of AlN particles(a)and AlN whiskers(b)formed when the Mg-Al alloy powder was burned in air
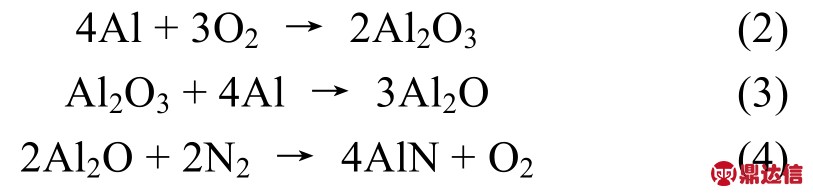
因此当镁铝合金在空气中燃烧时,镁的燃烧首先消耗掉氧气,使得在液态铝表面形成缺氧层,另外,即使有铝发生氧化,镁燃烧产生的热量也可以促使氮气与铝的氧化物发生置换反应,最终生成AlN。
镁铝合金在空气中燃烧时铝的氮化机理如图7所示。当温度上升到494.4 ℃左右时,分解产生的气态镁与空气中的氧气反应形成气相火焰。镁燃烧产生的热量不仅促进 Al12Mg17的分解,而且使铝熔化。如图6(b)所示,在氮化铝颗粒表面生成了大量的AlN晶须。根据Popenko等[14]研究,氮化铝晶须的形成主要有两种途径:气态铝的氮化或液态铝的氮化。由于镁铝合金在空气中的燃烧产物出现明显的分层,且由XRD检测结果可知,在上层白色氧化层中并未检测到单质铝或者氧化铝。说明在燃烧过程中,铝不太可能发生气相反应。液体铝的氮化在粒子表面形成一层致密的AlN保护层,大量的镁蒸汽聚集在保护层内,当其内压力达到临界值,保护层破碎,形成如图6(a)的小孔。高压的镁蒸汽向外扩散,一方面发生气相燃烧消耗掉氧气,另一方面使得空气中的氮气可以透过小孔进入到粒子内部,促进铝的氮化。镁蒸汽的扩散带动液体铝的流动,最终在粒子表面形成针状的AlN晶须。
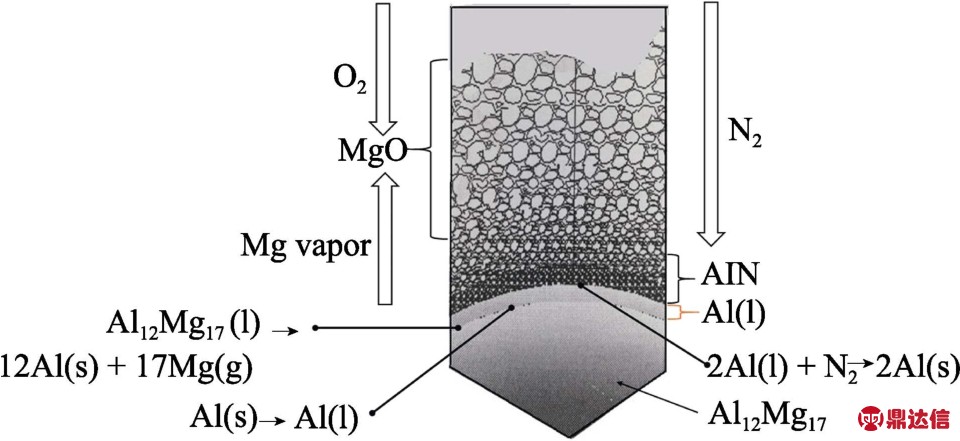
图7 镁铝合金在空气中燃烧合成AlN的机理
Fig.7 Synthetic mechanism of AlN by direct combustion of Mg-Al alloy in air
3 结论
以球形 Mg-Al合金粉(Al12Mg17)为原料,在空气中直接燃烧可合成高纯度的AlN晶体。相比于其它合成方法,镁铝合金点火温度较低(494.4 ℃),一旦被点燃,不需要外界热源的加热,燃烧产生的热量足以维持燃烧。燃烧产物由MgO和AlN组成,且出现明显的分层,上层为MgO,下层为AlN。合成过程中,镁与氧气的优先反应极大的促进了Al的氮化反应,使得合金中的Al可以全部转化为AlN。