摘要:使用沉淀沉积法及溶液浸渍法分别将Au和Pd纳米粒子负载在原子层沉积法制备的1cTiO2/SiO2载体上,制备出两种不同Pd 负载量的Pd-Au 双金属活性中心纳米催化剂。采用TEM、EDX、XPS 对所制备的催化剂进行了详细的表征,确定了纳米粒子的形貌、Pd-Au 元素的化学价态和组成。测试了该类催化剂在以氧气为氧源的环己烯环氧化反应中的活性和选择性,并对反应溶剂、共还原剂种类、反应温度等条件进行了筛选。在优化后的反应条件下考察了该催化剂对不同结构烯烃的适用性。对于环状烯烃,底物转化率均大于95%,环氧产物选择性均大于91%。催化剂在循环回收5次后,催化活性和反应选择性保持不变。
关键词:催化剂;纳米材料;环氧化;烯烃;活性;稳定性
引 言
烯烃是最重要的基础性化工原料之一,对其进行选择性氧化可得到醛、酮、醇和环氧化合物等高附加值的化学产品。其中,环氧化合物因其活泼的三元氧环结构,易发生开环反应,或与含醇、胺等官能团的化合物作用,广泛应用于精细化学品、食品添加剂、药物中间体和农药等生产领域[1-3]。目前,已有多种用于烯烃环氧化反应的氧化剂,如有机过氧酸[4-5]、叔丁基过氧化氢[6-7]、过氧化氢[8-12]和过氧化脲[13-14]等。氧气作为氧源具有价格低廉,易于获取,环境友好等优点[15-16],但分子氧需要在高效催化剂的作用下才能有效活化,并与C—H 键或C C 键反应。设计并合成高效且活化温度低的催化剂,是实现以氧气为氧源催化烯烃环氧化反应的关键。
贵金属在催化领域具有广泛的应用,纳米金催化剂在不饱和醛酮的选择性加氢[17]、水煤气变换反应[18]、烯烃的选择性氧化[19]等反应中表现出优异的催化性能。纳米钯催化剂已广泛应用于羰基化[20]、催化加氢[21]、氧化[22]等反应。Pd-Au 双金属催化剂与单独的Pd 或Au 催化剂相比,由于两种金属的合金化引起的团体效应和配体效应[23],金属纳米颗粒的尺寸更易控制,经常表现出更加稳定的催化性能[24-25]。
以SiO2分子筛等具有很大比表面的介孔材料为载体进行金属纳米颗粒的分散和负载,可以提高金属纳米颗粒的稳定性,减少贵金属的用量,同时也方便催化剂的回收。本文通过原子沉积技术在SiO2上沉积单层的TiO2薄膜得到1cTiO2/SiO2载体,再通过沉淀沉积法和溶液浸渍法将Pd-Au 双金属纳米颗粒负载在1cTiO2/SiO2表面,制备了Pd-Au/1cTiO2/SiO2催化剂并应用于以氧气为氧源的烯烃环氧化反应。通过单层TiO2对常规载体的修饰,使得催化剂表面金属纳米颗粒的尺寸均匀且高度分散,提高了贵金属的原子利用效率和催化剂的稳定性。单层TiO2修饰Pd-Au双金属催化剂用于以氧气为氧源的烯烃环氧化反应尚未见文献报道。
1 实验材料和方法
1.1 材料
异丙醇钛(RG,99.9%)、氢氧化钠(AR,99%)购自萨恩化学技术(上海)有限公司。三水合氯化金HAuCl4·3H2O(AR,99.99%),二水合硝酸钯Pd(NO3)2·2H2O (~40% Pd basis)购自Sigma Aldrich 公司,二氧化硅凝胶(S10040M,比表面积约为100 m3/g,粒径75~200 μm,孔径30 nm)购自Silicycle公司。以上试剂均直接使用,不再提纯。超高纯氮气(99.999%)购自南京天泽气体有限公司。
1.2 催化剂的制备
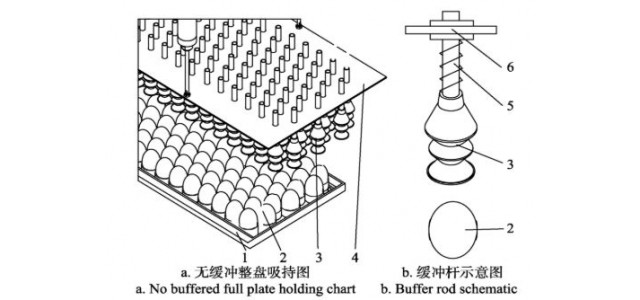
1.2.1 1cTiO2/SiO2 载体的制备 载体的制备使用Arradiance GEMStar-6原子层沉积系统,以二氧化硅凝胶(S10040M)为载体,异丙醇钛和H2O 分别作为Ti和O的前体源,超高纯氮气作为载气,载气进入原子层沉积系统前经Supelco气体纯化器进一步纯化。将0.5 g 预烘干的二氧化硅凝胶均匀地铺展到原子层沉积系统的反应器样品托盘上。在托盘顶部具有网罩防止样品掉出,但不影响前体和产物气体进出托盘时的有效扩散。TiO2的一个原子层沉积周期的时间序列可表示为t1—t2—t3—t4,其中t1和t3为两种前体的暴露时间,t2和t4为超高纯氮气吹扫时间。在473 K 温度下以时间序列为25 s—200 s—3.75 s—200 s交替暴露异丙醇钛和去离子水蒸气,在二氧化硅表面沉积单层TiO2。异丙醇钛储存在密封钢瓶中,并维持353 K的温度以便提供足够的蒸气压。
1.2.2 Au/1cTiO2/SiO2的制备 Au 纳米粒子通过沉淀沉积的方法负载在1cTiO2/SiO2载体上。将0.2 mg HAuCl4·3H2O 加入到100 ml去离子水中,再加入1 g 1cTiO2/SiO2载体。向上述溶液中逐滴加入1 mol/L的氢氧化钠溶液直至pH=7,滴加完毕后搅拌反应2 h。随后,过滤得到固体沉淀物质,并用50 ml 的去离子水洗涤,固体物质在室温下真空干燥过夜。
1.2.3 Pd-Au/1cTiO2/SiO2 的制备 Pd 纳米粒子通过水溶液浸渍的方法负载在Au/1cTiO2/SiO2上。分别将2 g Au/1cTiO2/SiO2置于浓度为0.18 g/L 和0.90 g/L 的2.8 ml Pd(NO3)2·2H2O 水 溶 液 中,用 于 合 成0.01%(质量分数,下同) Pd-Au/1cTiO2/SiO2和0.05% Pd-Au/1cTiO2/SiO2。浸渍后于室温下干燥1 h。最后,将样品置于50 ml/min 的125℃热空气流下干燥过夜。通过上述步骤制得的两种Pd-Au 双金属纳米催化剂,其Au 的负载量(质量分数)均为0.01%,Pd的负载量分别为0.01%和0.05%。
1.2.4 Pd-Au/1cTiO2/SiO2的还原 将上述制备的催化剂置于10%H2/He气氛下,在200℃下加热1 h。
1.3 表征测试仪器
采用日本JEOL 公司的JEM-200CX 型透射电子显微镜(TEM)拍摄样品的形貌,工作电压为100 kV,并测定其能量色散X射线光谱(EDX)。
采 用 日 本 UlVAC-PHI 公 司 PHI 5000 VersaProbe 型的X 射线光电子能谱(XPS)(X 射线源为Al Kα,真空度<10-10 Torr,1 Torr=133.322 Pa)进一步检测Pd-Au/1cTiO2/SiO2双金属纳米催化剂表面的元素组成及元素的价态。以结合能为284.6 eV 的C 1s峰为基准对结合能(±0.2 eV)进行校正。
1.4 催化剂的活性评价
向鼓泡式反应器中依次加入20 ml 溶剂、10 mmol 烯烃和10 mmol 共还原剂,再向反应体系中加入20 mg Pd-Au/1cTiO2/SiO2催化剂。将鼓泡式反应器置入恒温磁力搅拌器中,上端接入长度为700 mm的球形冷凝管,并利用循环冷冻泵通入-20℃的制冷剂进行冷凝,防止反应液被氧气带出。向鼓泡反应器中通入氧气,使用流量计控制氧气流量为50 ml/min,在40℃下反应4 h。采用对二氯苯为内标物,烯烃及其氧化产物的定量分析使用岛津公司的GC-2014C气相色谱进行,配置了HP-5弱极性毛细管色谱柱(30 m×0.32 mm×0.25μm)和氢离子火焰检测器(FID)。产物的结构使用岛津公司的GCMSQP2010气质联用仪进行鉴定。
气相色谱仪测试方法:气化室(SPL)温度为240℃,分流比为20;氢离子火焰检测器(FID)温度为250℃;色谱柱的初始温度为60℃(保持1 min),以15℃/min 的升温速率升至200℃(保持5 min)。色谱质载气为N2(≥99.9%),载气流速为1.25 ml/min。
烯烃转化率和产物的选择性采用式(1)、式(2)计算:

2 实验结果与讨论
2.1 催化剂的表征
2.1.1 催化剂的TEM 表征 图1 为Pd-Au/1cTiO2/SiO2的TEM 图,对于Pd 负载量较小的0.01%Pd-Au/1cTiO2/SiO2催化剂,Pd-Au 的颗粒感不明显,且金属颗粒上未发现明显的晶格条纹。对于Pd 负载量较大的0.05% Pd-Au/1cTiO2/SiO2催化剂,观察到明显的Pd-Au 颗粒,金属颗粒上具有明显间距为2.35 Å(1 Å=0.1 nm)的晶格条纹,与Au(111)晶面相匹配[16]。载体具有的层状结构为沉积的TiO2薄膜层。

图1 催化剂的TEM图
Fig.1 TEM images of catalysts
2.1.2 催化剂的EDX 表征 利用能量色散X 射线谱测定样品中所含的元素,并根据其强度测定元素的相对含量。从图2中可以确定样品主要含有的金属元素是Ti、Pd、Au,表明成功沉积了TiO2薄膜并负载了Pd 和Au。在Pd-Au/1cTiO2/SiO2 样品中,金属元素的摩尔比Pd∶Au∶Ti= 0.70∶0.70∶1.00,Pd 与Au的摩尔比为1.00。在0.05%Pd-Au/1cTiO2/SiO2 样品中,Pd∶Au∶Ti = 1.94∶0.38∶1.00,Pd 与Au 的摩尔比为5.11,这与在催化剂制备过程中控制的Pd、Au 摩尔比基本一致。
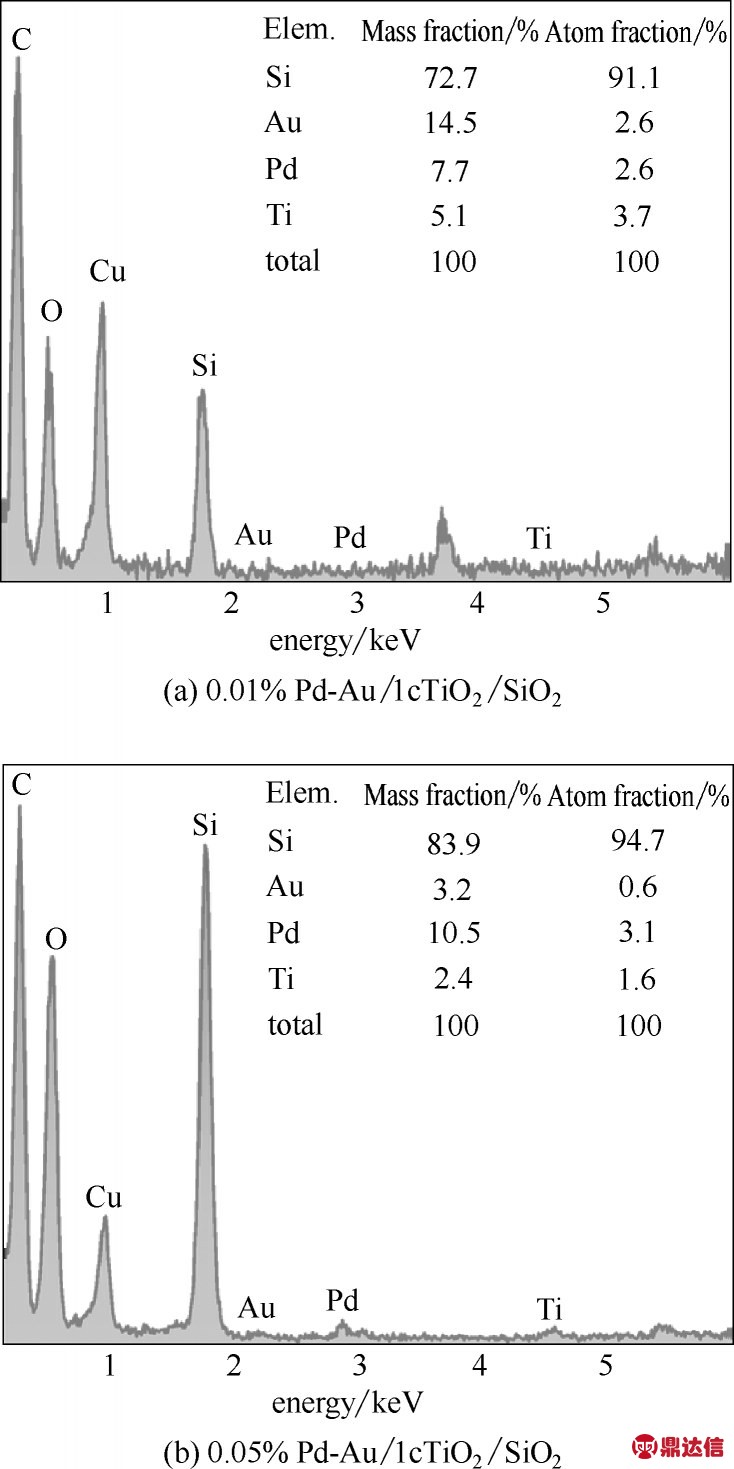
图2 催化剂的EDX能谱
Fig.2 EDX spectra of catalysts
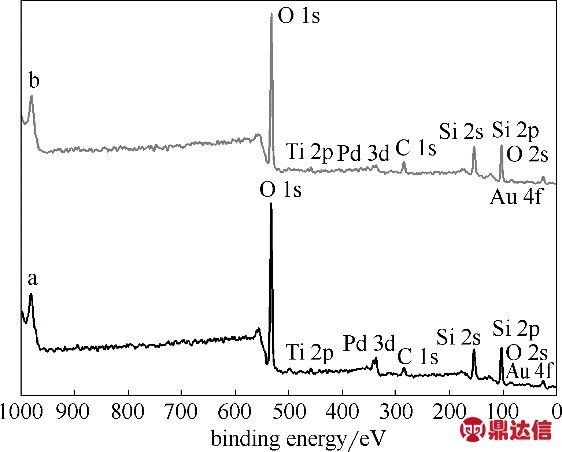
图3 催化剂的XPS宽谱
Fig.3 XPS wide scan spectra of catalysts
a—0.05%Pd-Au/1cTiO2/SiO2;b—0.01%Pd-Au/1cTiO2/SiO2
2.1.3 催化剂的XPS 表征 图3 为催化剂的XPS 宽谱,通过全谱扫描可初步判定催化剂表面的化学成分。在宽谱上,两种不同Pd负载量的催化剂均有相应元素的特征峰,其中C 1s 的结合能为284.5 eV,O 1s 和O 2s 的结合能分别为529.6 eV 和25.1 eV,Ti 2p 的结合能为458.6 eV,Pd 3d 的结合能为336.0 eV,Si 2s 和Si 2p 的结合能分别为154.2 eV 和101.6 eV,Au 4f 的结合能为84.4 eV。由于0.05% Pd-Au/1cTiO2/SiO2中的Pd 负载量较高,其Pd 3d 的峰强度明显要比0.01%Pd-Au/1cTiO2/SiO2的高。
图4 为催化剂的Pd 3d 和Au 4f 的高分辨谱,通过谱图可进一步确定催化剂表面Pd 和Au 的价态。对于0.01% Pd-Au/1cTiO2/SiO2催化剂,Pd 主要的化合价态为Pd2+和Pd0,Pd2+的结合能为336.86 eV(d5/2)和342.17 eV(d3/2) , Pd0的结合能为335.14 eV(d5/2) 和340.39 eV(d3/2)。Pd2+与Pd0的摩尔比为3.00。从图4(b)可以看出催化剂表面Au 主要的化合价态为Au0,其结合能为83.53 eV(f7/2)和87.16 eV(f5/2)。对于0.05%Pd-Au/1cTiO2/SiO2催化剂,其Pd2+的结合能为337.41 eV(d5/2) 和342.65 eV(d3/2) , Pd0 的 结 合 能 为336.78 eV(d5/2) 和342.05 eV(d3/2),Au0 的 结 合 能 为83.58 eV(f7/2)和87.26 eV(f5/2)。且Pd 负载量的增加导致Pd2+与Pd0的摩尔比由3.00 降至0.94。标准数据库中PdO 的结合能为336.90 eV(d5/2) 和342.20 eV(d3/2);Pd 单质的结合能为335.08 eV(d5/2)和340.30 eV(d3/2);Au 单质的结合能为84.0 eV(f7/2)和87.7 eV(f5/2)。上述两种催化剂表面的Pd2+和Pd0的结合能相比于PdO 和Pd 单质均有小幅度的增加,可能是Pd 纳米颗粒上部分电子转移至TiO2上,导致Pd电子云密度稍有降低,结合能变大。同理,催化剂表面的Au0结合能相比于单质Au 稍有降低,可能是Au 纳米颗粒与TiO2的界面处形成了肖特基势垒,TiO2上的部分电子迁移到了Au 纳米颗粒上,导致Au 电子云密度稍有增加,结合能变小[26-28]。
2.2 催化剂催化环己烯环氧化反应活性评价
对催化活性的评价,以环己烯为反应物,氧气(O2)作为氧化剂,异丁醛(IBA)作为共还原剂,环己烯环氧化反应的目标产物是环氧环己烷(CHO),副产物为2-环己烯-1-醇(cyol)和2-环己烯-1-酮(cyone),如图5 所示。图6 则显示了不同催化剂的催化活性。当催化剂中Pd负载量增加时,环己烯转化率会得到明显提升,但对产物选择性几乎没有影响。这说明Pd 负载量的提高导致Pd2+与Pd0的摩尔比下降,这种催化剂结构的变化导致了环己烯催化活性的提升,大幅提高了环己烯的转化速率和最终转化率。在不加入异丁醛共还原剂时,主要发生烯丙基氧化反应,烯丙基位氧化产物cyol和cyone的总选择性高达97%,环氧化产物的选择性仅为3%,且环己烯转化率也有大幅下降。在无催化剂参与反应时,环己烯也能高选择性地转化为环氧环己烷,但其反应速率较慢。在以氧气为氧源的烯烃环氧化反应中,自由基链反应机理已被广泛接受[29-31]。氧气吸附在金属催化剂表面生成过氧自由基,过氧自由基再将异丁醛转变为过氧异丁酸自由基,过氧异丁酸自由基与异丁醛作用生成过氧异丁酸。过氧异丁酸可将活性氧原子转移至烯烃双键上,使烯烃环氧化生成环氧化合物,异丁醛最终转变为异丁酸。因此,Pd-Au/1cTiO2/SiO2催化剂和共还原剂在环己烯环氧化反应中都起到了关键作用。
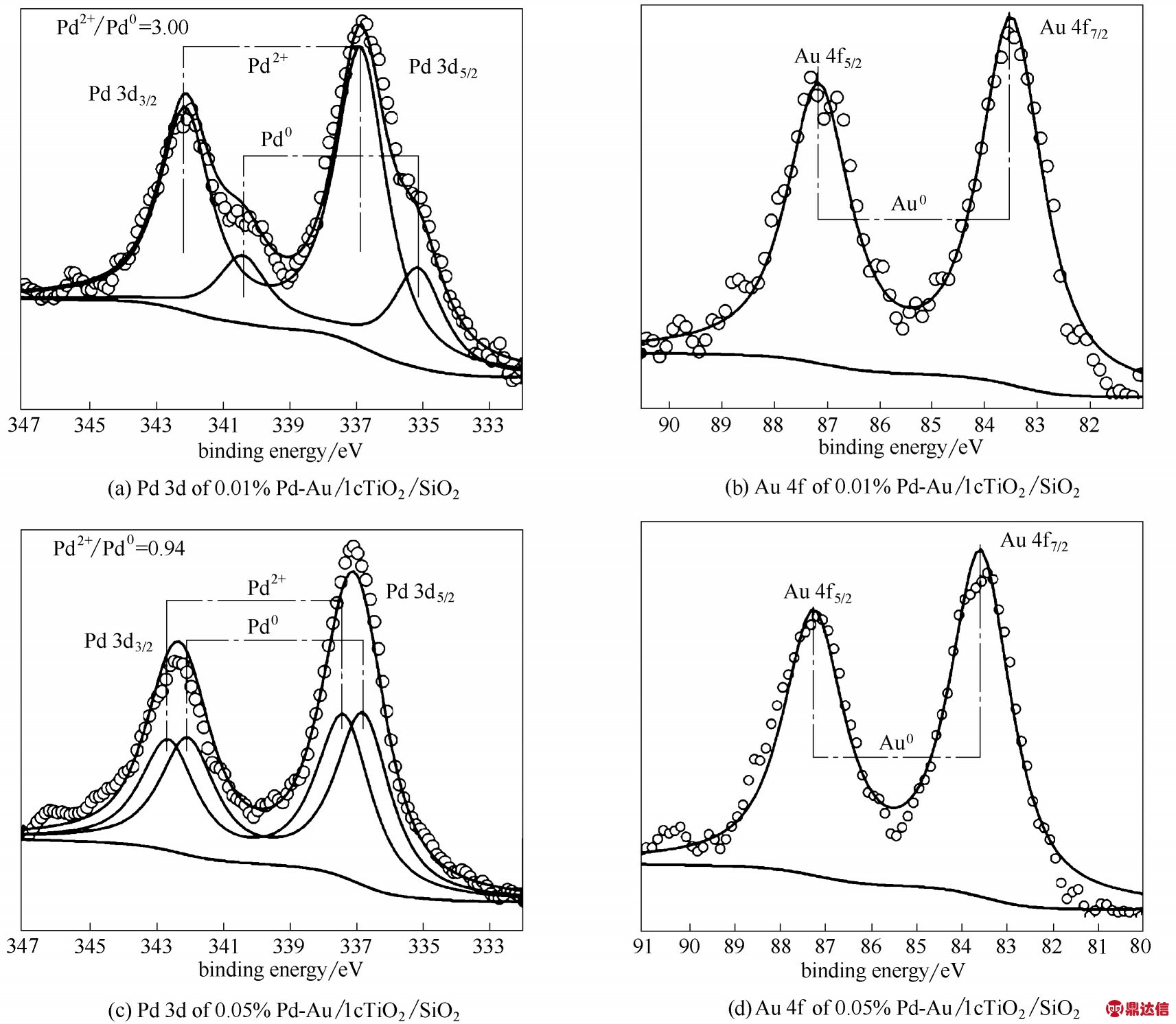
图4 催化剂的XPS高分辨谱
Fig.4 XPS core level spectra of catalysts
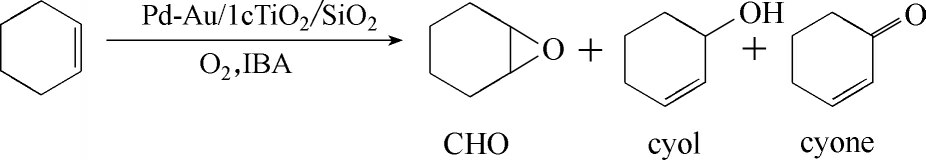
图5 环己烯环氧化反应
Fig.5 Epoxidation of cyclohexene
2.3 反应条件的影响
在比较了不同催化剂的催化活性后,选取活性更高的0.05% Pd-Au/1cTiO2/SiO2为催化剂,考察了溶剂种类、共还原剂种类和反应温度对反应转化率和选择性的影响。
2.3.1 溶剂种类的影响 图7所示是溶剂种类对环己烯环氧化反应的影响。当以甲醇为溶剂时,环己烯转化率为12%,且环己烯主要是烯丙基位发生氧化反应,环氧环己烷选择性仅为12%。乙醇和四氢呋喃为溶剂时,环氧环己烷的选择性均小于55%。氯代烃和丙酮为溶剂时,环氧环己烷选择性大于80%,但环己烯转化率较低。乙腈为溶剂时,环己烯转化率超过99%,环氧环己烷选择性可达86%。值得注意的是,在质子型溶剂(甲醇,乙醇)条件下的催化剂活性最低;在非质子型溶剂中,随着溶剂极性的逐渐增大(二氯甲烷(3.4)<四氢呋喃(4.2)<氯仿(4.4)<丙酮(5.4)<乙腈(6.2)),环己烯转化率基本呈现出增加趋势(二氯甲烷(26%)<氯仿(29%)<四氢呋喃(32%)<丙酮(53%)<乙腈(99%))。Payne等[32]报道了腈类物质在烯烃环氧化反应中起到了共反应物的作用,其可在氧化剂作用下生成亚氨基过氧酸,亚氨基过氧酸将活性氧转移至烯烃生成环氧化合物和酰胺化合物。在Pd-Au/1cTiO2/SiO2催化的环己烯环氧化反应液中,通过GCMS 并没有检测到乙酰胺的生成,说明乙腈没有作为共反应物参与反应,可能是乙腈的极性非质子型溶剂性质和低配位能力对Pd-Au/1cTiO2/SiO2 的催化活性起到了促进作用。
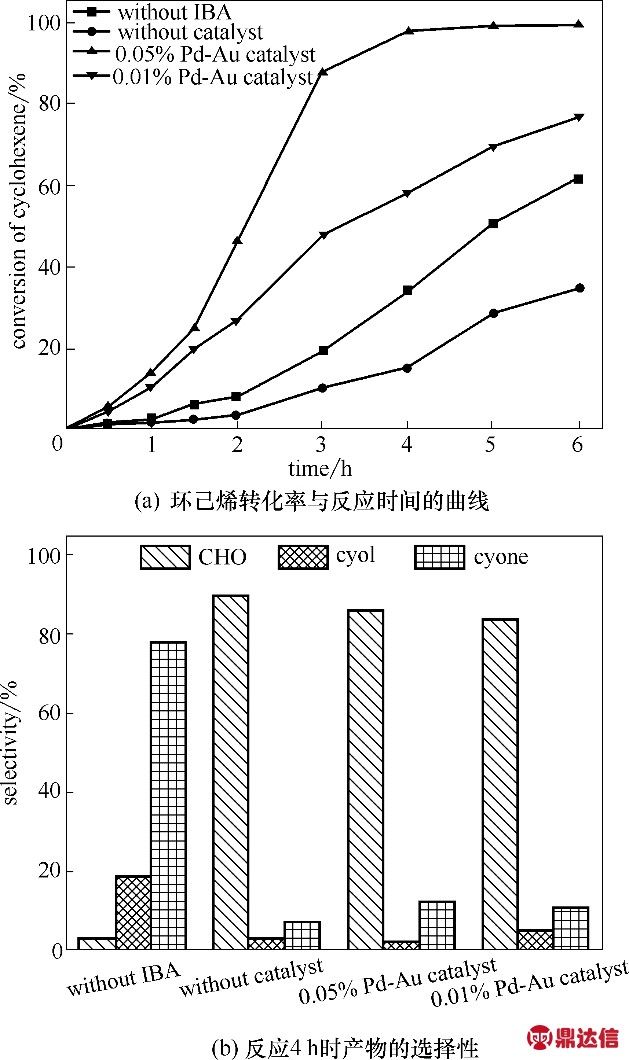
图6 不同催化剂反应活性的评价
Fig.6 Performance of different catalysts
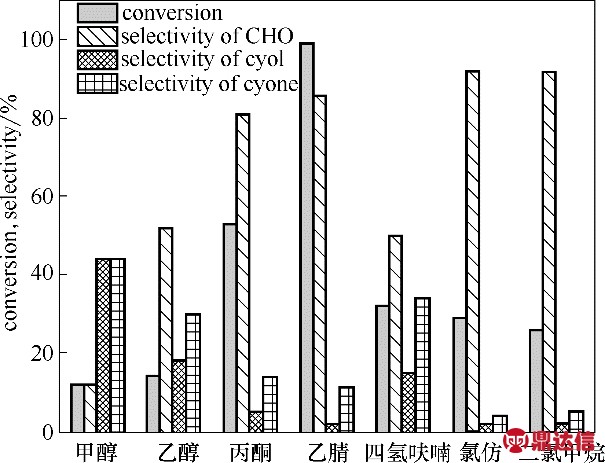
图7 溶剂对环己烯环氧化反应的影响
Fig.7 Effect of solvent on epoxidation of cyclohexene
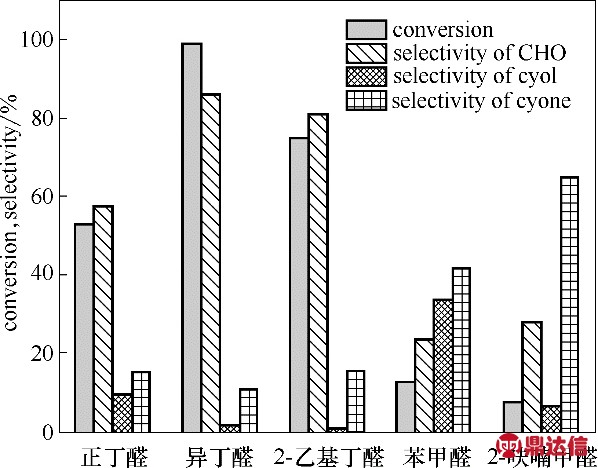
图8 共还原剂对环己烯环氧化反应的影响
Fig.8 Effect of co-reductant on epoxidation of cyclohexene
2.3.2 共还原剂的影响 共还原剂的加入可协助催化剂激活氧分子,生成含活性氧的过氧化合物,可显著提高环己烯的转化率和环氧环己烷的选择性。如图8 所示,考察了5 种不同的醛作为环己烯环氧化反应的共还原剂时的催化活性。以苯甲醛、2-呋喃甲醛作为共还原剂时,主要以烯丙基位氧化产物为主,且环己烯的转化率也很低。异丁醛作为共还原剂,可以获得最高的转化率(99%)和环氧环己烷选择性(86%),因此,选用异丁醛作为最适合的共还原剂。
2.3.3 反应温度的影响 反应温度对环己烯环氧化反应的影响如图9 所示,随着反应温度从20℃升至40℃,环己烯的转化率由30%逐渐升高至99%,环氧环己烷的选择性随温度升高而稍有增加。温度从40℃进一步升至50℃,产物选择性没有明显变化,这表明反应体系的操作温度以40℃左右为宜。
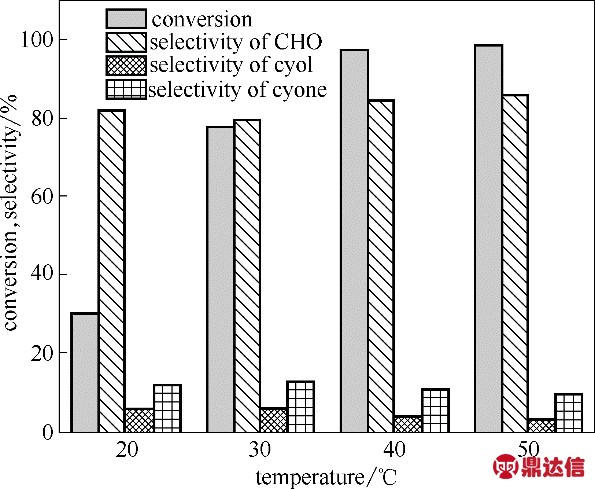
图9 反应温度对环己烯环氧化反应的影响
Fig.9 Effect of reaction temperature on epoxidation of cyclohexene
2.4 催化剂的回收性能
催化剂的回收性能是决定催化剂是否具有应用潜力的重要参数,选择优化后的反应条件进行0.05% Pd-Au/1cTiO2/SiO2 催化剂的回收稳定性测试。对于负载型的Pd-Au 双金属纳米催化剂,其回收操作简单。在反应结束后,将反应液转移至离心管中离心,去除上层清液,再以40 ml 乙酸乙酯分四次洗涤固体沉淀物,最后将回收的催化剂置于50℃的真空干燥箱中8 h。在相同的反应条件下,采用回收的催化剂重复实验,无需补偿新鲜催化剂。如图10所示,0.05%Pd-Au/1cTiO2/SiO2催化剂循环使用5次,环己烯的转化率和产物的选择性没有明显的变化,这说明Pd-Au 双金属纳米催化剂具有良好的回收性能。
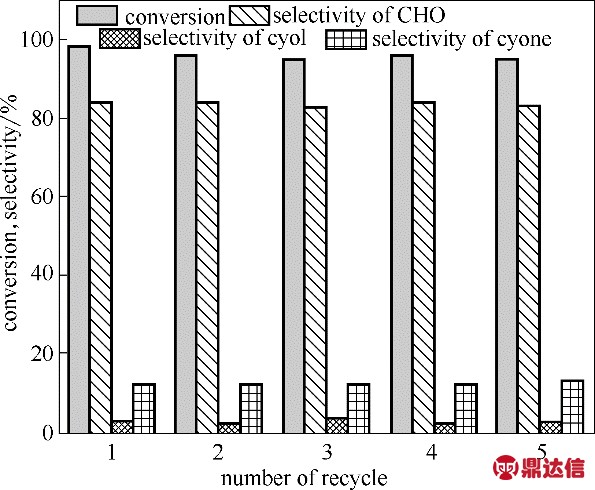
图10 0.05%Pd-Au/1cTiO2/SiO2催化剂的回收性能测试
Fig.10 Reusability of 0.05%Pd-Au/1cTiO2/SiO2 catalyst
2.5 反应底物的拓展
如表1 所示,选取了10 种不同化学结构的烯烃进行环氧化反应,以考察催化剂对不同烯烃的的适用性。Pd-Au双金属纳米催化剂对于环状烯烃的催化活性较高,烯烃转化率均大于95%,环氧化产物选择性均大于91%。但该催化剂对于直链烯烃的催化活性较低,在延长反应时间并增加催化剂用量的条件下,直链烯烃的转化率均小于60%。
表1 不同烯烃的环氧化反应
Table 1 Epoxidation of different olefins catalyzed by Pd-Au catalyst
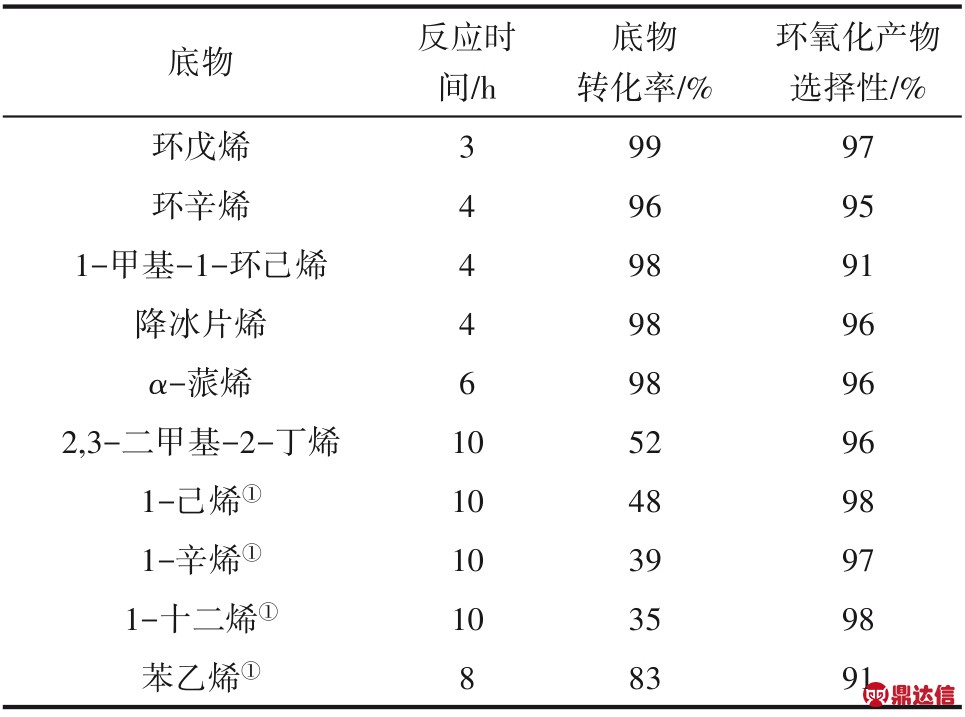
注:乙腈20 ml,底物10 mmol,异丁醛10 mmol,0.05%Pd-Au/1cTiO2/SiO2 20 mg,O2 50 ml/min,反应温度40℃。
①0.05%Pd/Au/1cTiO2/SiO2 40 mg。
3 结 论
采用原子层沉积方法制备了单层TiO2修饰的SiO2载体,运用沉淀沉积法和浸渍法制备了两种不同Pd 负载量的催化剂0.01% Pd-Au/1cTiO2/SiO2 和0.05% Pd-Au/1cTiO2/SiO2,通过TEM、EDX 及XPS 表征表明了Pd负载量会影响催化剂表面的形貌、元素化学价态及组成。
以环己烯环氧化为探针反应,对反应的溶剂、共还原剂种类及用量、催化剂用量、反应温度等反应参数进行了详细的优化。乙腈是最优选的溶剂,异丁醛作为共还原剂的环氧化反应效果最好。Pd负载量的增加,改变了催化剂的形貌和结构特征,使得催化剂的活性增加,使得环己烯反应速率显著提升,但环己烯的氧化产物的分布变化不大。Pd-Au 双金属纳米颗粒具有很好的稳定性和可回收能力,催化剂回收5次,催化活性和反应选择性几乎维持不变。
通过底物拓展实验验证了催化剂对不同烯烃具有广泛的适应性, 对环状烯烃、催化活性和环氧产物的选择性均在91%以上,但对直链烯的催化活性较小,直链烯烃转化率不到60%。Pd-Au 双金属纳米催化剂能够成为环状烯烃选择氧化的高效催化剂,有很好的应用前景。