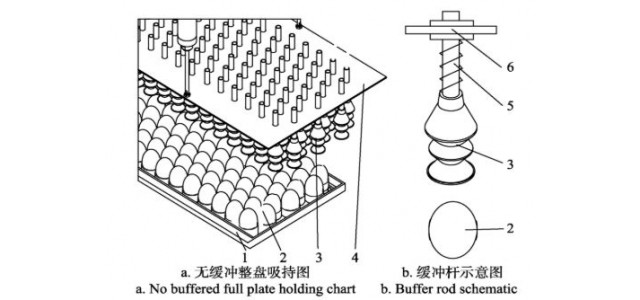
摘要:人脑与电脑通过连续高通量的信息交互来实现深度融合是神经工程领域的重要发展愿景。脑机融合技术不但可以大幅提升运动残障、精神疾病、感知觉缺失能等多种疾病患者的治疗效果,更可以将电子计算机系统中存储的海量信息以及高速数值计算能力直接传递给人脑,从而赋予个人“超能力”。植入式神经电极阵列是发展宽带脑机融合智能系统所不可或缺的关键界面器件。一方面,植入式电极阵列可以同时保证大范围和高精度地记录神经元动作电位的精确发放时间和波形,为充分抽提神经信息,解读脑神经网络的活动奠定坚实基础。另一方面,借助植入式电极阵列对神经元进行高时空精度地信息写入,不但可以向脑内直接传入新信息,也可能改变神经精神疾病(例如帕金森氏症、癫痫和重度抑郁等)患者的异常神经网络活动,从而缓解症状或治疗疾病。电极阵列的微纳加工工艺、电极的理化特征及其与神经组织的界面效应是目前脑机接口技术前端研究的重要方向,而纳米材料和纳米器件等新技术在神经电子界面优化方面的重要作用也愈发明显。
关键词:脑机接口;生物电子医疗;多电极阵列;在体电生理;纳米材料
1 引言
人类大脑中的大约1000亿个神经元之间通过复杂的动作电位传递信息1,而这些电活动参与了感知觉产生、运动编码和高等认知等脑功能产生过程。神经工程学集合了神经科学、控制科学、电子工程、材料学、应用数学和物理学等众多学科的科学家和工程师,试图理解意识和行为产生的电活动机制,并利用调控手段和假体等实现对神经缺损功能的修复和脑认知能力的提升。迄今,神经工程学已经通过技术进步造福了大量患者,例如人工耳蜗修复听力缺损已经造福了超过30万患者2,深部脑刺激已经帮助超过10万的帕金森、肌张力障碍、特发性障碍,甚至Tourette综合征和强迫症患者3,人工视网膜也已经帮助数百位视觉损伤患者重见光明4,而脑机接口控制的机械手帮助高位截瘫患者重获运动和外界交互的能力的案例在中外均已有所报道5。近期,利用神经工程方法,科学家甚至可以让患阿尔兹海默症的小鼠恢复部分记忆6,这项技术未来可能造福大量患者,甚至帮助人们实现超快速学习。
由于脑技术的重要性,奥巴马执政美国期间,国立健康研究院(NIH,National Institutes of Health)提出了脑计划(BRAIN Initiative,Brain Research through Advancing Innovative Neurotechnologies),全称为基于创新性神经科技发展的脑研究计划7。此后美国国防部高级研究计划局(DARPA,Defense Advanced Research Projects Agency)推出了神经工程系列研究项目,欧洲推出了人脑研究计划,日本也推出了脑图谱研究计划8。值得一提的是,2019年11月,美国陆军作战能力发展司令部向美国国防部提交了《2050年机械战士:人机融合与国防部的未来》报告,提到的4大变革性技术:脑机接口、视觉增强、听觉增强和外骨骼战斗服这些方向均与神经技术发展存在诸多联系。如图1B,DARPA早在1970年代就已经关注神经系统,此后一直在发展、新增诸多神经技术项目,图中标识了各项目启动的年份或年代,字体颜色标识是否植入,背景颜色标识项目的目标领域,其中白色背景为通用技术,不指向单一目标领域。2016年,DARPA分别启动了“神经工程系统设计”(NESD,Neural Engineering System Design)项目,旨在研究士兵直接连接电脑的侵入式脑机接口;“革命性义肢”(Revolutionizing Prosthetics)项目,旨在开发可使士兵用脑控制装置的技术。2017年的“重建主动记忆”(RAM,Restoring Active Memory)项目,旨在研发非侵入式新型脑机接口;2018年的“下一代非侵入性神经技术”(Next-Generation Nonsurgical Neurotechnology,N3)项目,旨在研究脑中多位点同时读写而实现人机多任务协同;2019年的“沟通+”(Bridging the Gap Plus,BG+)项目,首次扩展到脊髓接口,丰富了神经控制途径,或可使士兵通过神经控制多设备。DARPA通过这些项目,使脑机接口从有创、单任务、脑界面向精创、多任务、脊髓界面等方向不断进步。美国DAPRA与国防部门对这些研究的重视,一方面显示了脑机接口材料与器件研究在未来各种场景均可发挥至关重要的作用,另一方面也显示了美国试图在该领域竞争中建立绝对技术优势的理念和决心。
特别是近几年,Neuralink公司凭借其创始人Musk的知名度而备受关注。脑机接口作为该公司商业计划的核心技术而成为关注焦点。该公司提出的脑机接口设想是使用数千上万通道的微纳加工电极阵列制成脑机通讯界面9,从而进行脑信息的高通量读取与写入。该技术采用的电极阵列的柔性电极导线和缝纫机式自动化植入方法在临床应用方面有较好的前景,而且该植入式电极阵列设计已经被证实具有较好的稳定效果9。值得提及的是Neuralink目前公开展示的所有分项技术均来自学术领域已发表的研究成果,但在展示中实现的电极通道数、系统集成度以及信号传输带宽等方面均进行了工程优化,神经信息通量(约3000道)远高于传统FDA (Food and Drug Administration)认证的人体可用的犹他电极(约100道)。Neuralink系统为脑机接口的界面交互能力带来了整体的提升。虽然目前Neuralink尚未展示对神经信息实时解码的计算能力,但神经信息通量的大幅提升已经预示着脑机接口应用场景将发生质变的趋势。
对神经电信号的记录与调控是离不开多电极阵列装置的,而传统的金属微丝阵列或硅基阵列均可用于记录场电位和动作电位信号。在神经元功能的研究与调控方面,多电极阵列在过去二十年内取得了众多材料与器件方面的突破。同时,神经影像、分子遗传、显微成像等技术的进步也已经在脑认知与疾病机制的研究中取得了一系列重要的进展,与这些新技术的联合有望产生更多原创新突破。但目前的神经电极界面技术无论在体内神经环路研究、生物电子医疗还是脑功能调控等方面都面临着重大挑战,也伴随了大量机遇。目前的体内多电极阵列技术,正在向超高密度记录、大范围记录、创伤微小化、慢性生物相容性、无线高通量采集与调控等众多新型高性能界面技术与材料方向发展,但目前的技术通常针对某一特点做深入地改进却不能提高整体器件的应用效果。本文将针对目前体内多电极阵列技术的发展情况进行综述,并分析未来可实用化的电极技术需要具备的技术特点。
2 不同尺度神经电信号记录原理
在体胞外记录的电信号包括低频(主要为0-100 Hz)的局部场电位(LFP,Local Field Potential)和高频的动作电位(如图1A)。LFP反映了一定范围内神经元膜电位总和,而数百Hz到约3000 Hz的带通滤波后的信号则包含了动作电位的波形。记录到的动作电位波形一般又可分为单神经元活动(SUA,Single Unit Activity)和多神经元活动(MUA,Multi-Unit Activity),这些动作电位发放的时空特性编码了大量信息。
相对低频的场电位在脑区之间信息传递和同一个脑区内部的神经元之间通过锁相而进行同步化发放的过程中发挥重要作用10,其特定频段也可以反映一定范围神经元网络在大脑清醒、思考、睡眠、癫痫发作等不同状态下的活动特征。例如,海马中4-8 Hz的theta波以及与theta周期锁相的神经元动作电位发放可能在记忆的形成和突触可塑性方面发挥了重要的作用11。
神经系统中独立的功能与结构单元为神经元,因此在体电生理实验中记录单个神经元活动对理解大脑信息处理机制至关重要12。各种植入式高通量神经界面技术的重要评判标准之一即对胞外动作电位记录中的动作电位数量和信噪比,比起膜片钳技术一次只能记录一个细胞,胞外电生理电极一般可以记录到50 μm半径内的动作电位甚至140 μm范围内神经元的活动13。通常同一个通道记录到的不同神经元来源的动作电位波形不会完全相同,这样可以分析出波形不同的多个SUA 14,即动作电位分拣(Spike Sorting),也有很多研究直接采用MUA进行后续发放频率计算15。间距很近的胞外记录电极组,例如四极电极和高密度密歇根电极等,可以实现对同一个神经元活动的多位点采集,这样可以通过更多的波形信息更好地区分多个来源的神经元信号14,16。
神经电信号最早由意大利科学家Galvani 1采用早期的电极技术记录到。随后,Hodgkin和Huxley成功地从0.5-1 mm宽的大王乌贼轴突中检测到神经活动17,进而根据这些电信号的记录发展出了经典的膜电位理论基础。1957年,Hubel 18通过亚微米直径的钨丝尖电极成功地从哺乳动物猫脑中极小尺寸的神经元和轴突中记录细胞外动作电位,而这项发明在神经科学和神经工程领域都产生了深远的影响。这些电极帮助Hubel和Wiesel 19在视觉神经生理学方面做出了开创性贡献,并引导了新型胞外电生理信号记录探针技术的发展,从四极管电极20到微加工硅密歇根微电极阵列21和犹他微电极阵列22等。
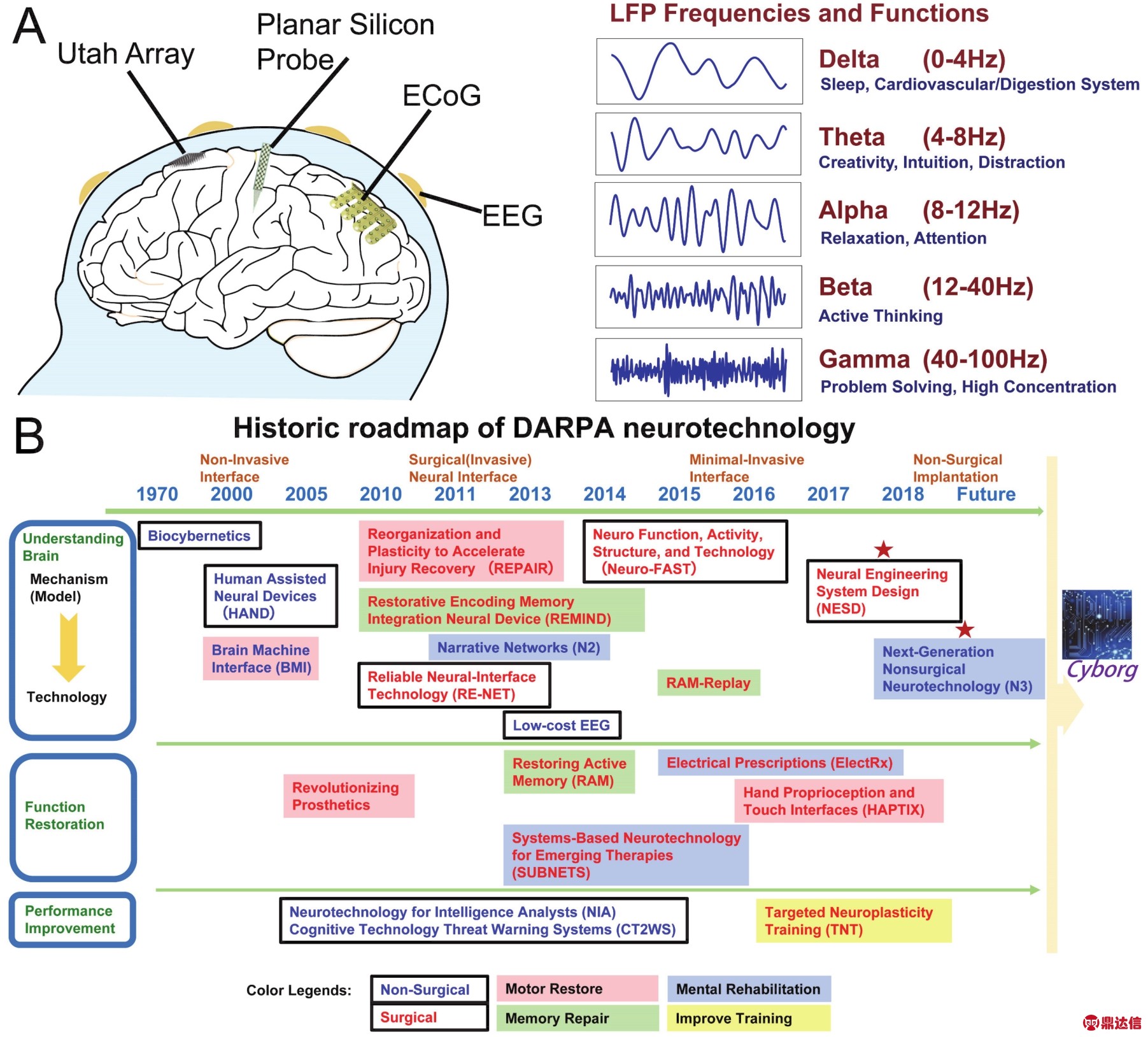
图1 在体神经界面与美国国防部高级研究计划局神经科技项目群的发展历程
Fig.1 In vivo neural interface and historic roadmap of DARPA neurotechnology.
(A)Neural interface electrode types and neural oscillation frequency band functions (ECoG,Electrocorticography; EEG,Electroencephalogram);(B)Historic roadmap of DARPA neurotechnology projects.
在半导体产业迅猛发展的今天,神经电极技术,包括很多基于微纳加工的电极阵列技术,却长期受到发展缓慢的限制,反映了本领域经济驱动和产业支撑相对匮乏对技术进步带来的限制,这些原因主要可以总结为三个方面。首先,电极采样体积需要尽可能大才能全面理解神经网络的信息加工,但多点、大范围地侵入式采样难免造成更严重的神经损伤23,而成年动物的脑组织再生能力极弱并局限于很小范围。其次,设备无论是有线还是无线的输入/输出接口及信号采集/转换设备都受到加工精度、尺寸、重量等多方面限制。而且,电极密度、精度的提高势必要求尺寸的减小,但微小的金属电极触点会带来严重的阻抗升高,进而提高采集系统的噪音,降低信噪比,造成难以调和、互相矛盾的需求24。针对这些难点,现在已经有很多材料、器件方面的研究尝试对兼具记录与刺激功能的双向神经界面技术进行改进,其中记录功能可以实现运动解码或疾病环路监测、解析,而刺激功能可以实现感觉反馈或感知觉替代、疾病干预,以下将对近期科研领域的进展做详细综述。
3 在体神经电极阵列材料与器件
3.1 在体电极阵列新技术
传统胞外记录采用的钨丝电极等低通道数的记录为神经科学的发展提供了重要的工具25,但与目前快速发展的影像学及钙荧光和电压敏感蛋白成像26等神经技术相比,这些简单的胞外电生理器件已不能在时空尺度、分辨率和多元复合功能等方面提供足够的信息27。
高通量的神经记录可以采集更多的神经元从而利于整体解码体内神经元网络的功能产生机制,同时为脑机接口技术提供更多数量的控制自由度和鲁棒性。在传统的基于微纳刻蚀技术的密歇根电极基础上,可以直接增大电极密度,减小尺寸从而增加通道数,这类新型电极阵列的代表是Neuropixels 28 (如图2G,2J),Neuroseeker 29和3D(Three dimensional)silicon probe 30。Neuropixel电极有966个记录通道,每个通道12 μm × 12 μm大,间距25 μm,采用130 nm的CMOS (Complementary metal-oxide-semiconductor)技术加工,整个电极阵列长10 mm,宽70 μm,这种电极阵列有384个记录通道,而记录通道与电极位点的对应关系可以由硬件编程控制。在小鼠脑中植入2个Neuropixel电极,可以在5个脑区采集700个以上的神经元活动28。Stringer等31通过Neuropixel电极和钙荧光记录,实现小鼠头面部肌肉的自发运动模式与小鼠全脑大规模神经活动的相关性分析。
为了提高生物相容性,实现长期稳定的神经记录,Liu等23a开发了一种类神经组织的网状电极列。构成这种电极的线尺寸小于神经元的胞体直径,而且在大尺度的网孔间隙允许神经元突触连接生长穿过这种电极阵列,而小尺寸的电极材料也尽量避免了炎症信号分子在电极表面的聚集导致的胶质细胞反应恶化32。例如Wei等33开发的微小柔性高密度电极(如图2H)和Yang等34开发的仿神经元电极(如图2M)等都尝试针对这些技术难点进行突破。这种网状神经电极通过类似密歇根电极的微纳加工方式产生二维结构后,可以通过注射方式植入脑中时扩散形成三维空间的覆盖35。Guan等36开发的神经流苏电极也可以实现在植入后展开从而对较大范围的神经元开展研究(如图2E)。Du等37的研究证实,这类柔性神经电极材料可以降低电极尖端微扰动等带来的组织炎症反应,从而在一年以上的时间尺度内记录神经元的活动38。
为理解产生特定脑功能的细胞群体的活动规律,需要同时记录大量的神经元放电,然而由于脑内神经元的密度很高,在记录尽量多的神经元同时,也要求植入神经器件尺寸较小。由于近年来半导体产业微纳加工能力的突飞猛进,目前在高密度神经电生理采集的器件加工方面也有较多进步。
Neuroseeker电极也是用130 nm的CMOS技术生产的电极数达到1344个的电极阵列,也是目前是通道数最多的电极阵列。单个Neuroseeker电极长度为8 mm,因此可以同时记录感觉皮层、海马和丘脑的场电位和动作电位29。尽管这两种电极阵列可以应对高密度记录和深度记录的挑战,但由于密歇根电极类器件加工的限制,它们在水平尺度大范围记录方面不能提供很好的方案。结合了犹他电极和密歇根电极优势的3D硅电极阵列,在4行4列排布的16根电极体上每个都有64个电极位点。另外,由于3D硅阵列的切换电路也就是产热部分是在颅骨外部附着的,因此可以较好地应对产热对神经活动和神经元存活率可能产生的负面作用30,39。
这些可以进行深部采集的电极阵列通常要面临脑组织损伤的问题40,而为了减小神经元受到的损伤,硬脑膜下多电极阵列也可以记录到较好的胞外电信号(如图2A)。例如一种柔性360通道的电极阵列40b可以在猫的大脑皮层上覆盖10 mm × 9 mm的范围,并采集睡眠、视觉任务以及癫痫发作等不同状态下皮层的活动41。由于这类电极的水平覆盖范围很大,每个电极尺寸为300 μm × 300 μm,这些电极记录的信号无法分离出SUA,但可以分析脑表面电位的传播方向等信息,并且新一代NeuroGrid阵列上的10 μm × 10 μm尺寸的电极已经很接近神经元的胞体尺寸(10-20 μm直径),这类电极已经可以同时记录场电位和动作电位42。而Zhang等43开发的透明可拉伸电极阵列则可以实现光遗传调控与电生理记录等功能(如图2K,2N)。同时Hong等44开发的柔性电极阵列也可以记录视网膜上的SUA(如图2L)。
由于Neuropixel类电极阵列可以同时记录多个深度的不同脑区且在每个脑区都可以记录大量的神经元,因此可能实现对兴奋神经网路空间尺度较好地估计。而NeuroGrid类的电极阵列可以对多个表面脑区的功能进行定位。因此结合这两类电极阵列可以实现广度和深度同时兼顾的神经信号采集45,甚至可能观察到复杂的认知行为对应的电生理基础,例如复杂脑网络的动力学特征46和记忆信息在不同脑区之间的传递规律47。Chung等48开发的1024通道聚合物电极针对电极通道数与记录范围不足的问题开发了一种较好的电极阵列(如图2B,2C)。
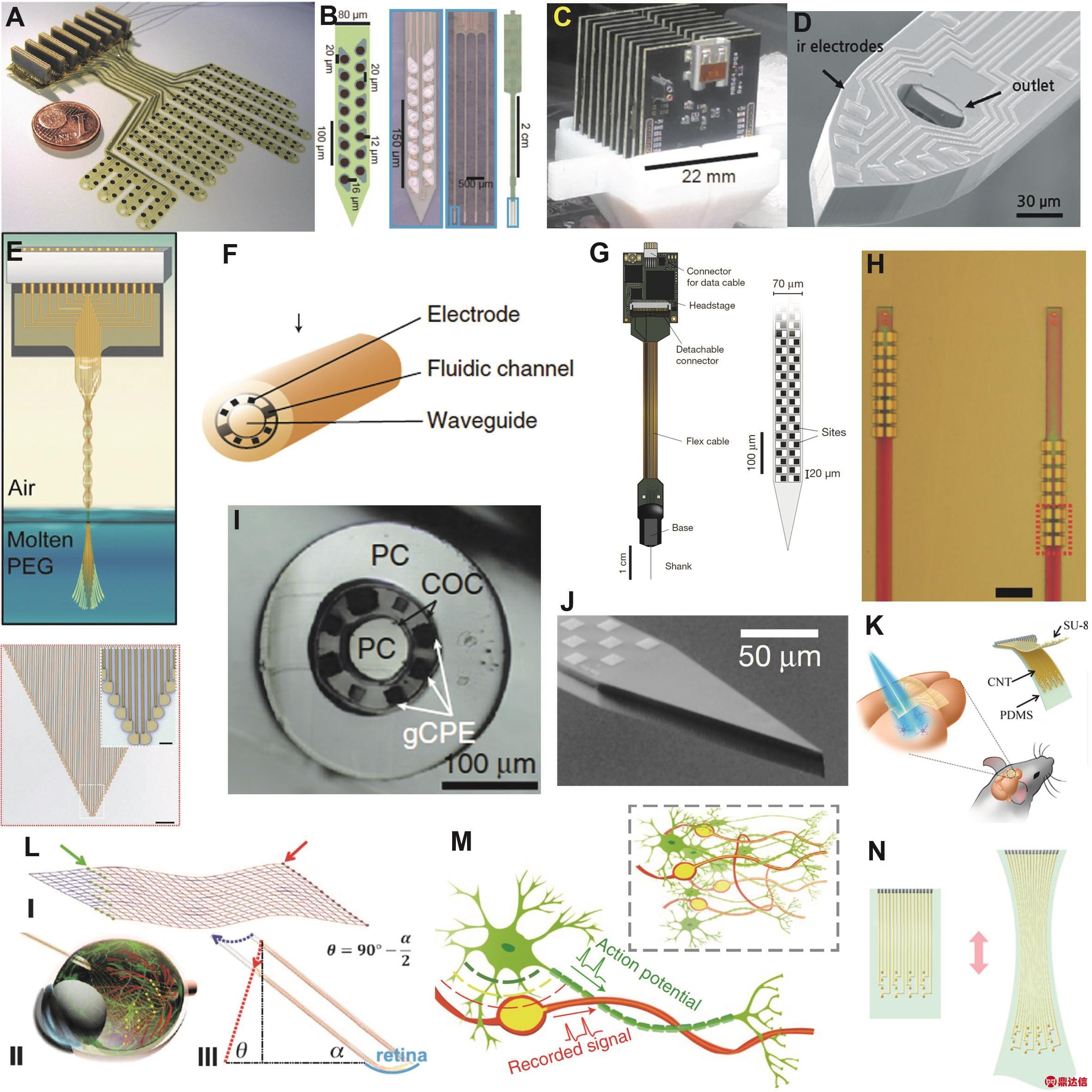
图2 微纳加工电极阵列与器件
Fig.2 MEMS (Micro-Electro-Mechanical Systems)fabricated electrode arrays and devices.
(A)High density grid ECoG recording electrode array 40c; (B)High-density polymer electrode array 48; (C)Recording setup of 1024 channel polymer array 48;(D)Microfluid and electrophysiology electrode array 55; (E)Neurotassl electrode array (PEG,Polyethylene glycol)36; (F)Multi-functional fiber 54;(G)Neuropixel electrode array 28; (H)Ultraflexible high-density electrode array 33; (I)Cross-section of multi-functional fiber device (PC,Polycarbonate;COC,cyclic olefin copolymer;gCPE,graphite-conductive polyethylene)54; (J)SEM(Scanning Electron Microscopy)of neuropixel electrode 28;(K)Transparent stretchable electrode array 43; (L)Retina implantable electrode array 44; (M)Neuron-like electrode array 34; (N)Stretchable electrode array 43.(A,B,C)Reprinted with permission from Elsevier.(D)Reprinted with permission from Royal Society of Chemistry.(E,L)Reprinted with permission from The American Association for the Advancement of Science.(F,G,I,J,M)Reprinted with permission from Springer Nature.(H)Reprinted with permission from John Wiley and Sons.(N,K)Reprinted with permission from American Chemical Society.
随着微纳加工电极阵列的密度与精度的提升,伴随着电极接触面积减小带来的电极阻抗升高带来一定的噪音升高和信噪比的降低,通过增加表面褶皱结构、多孔结构或其他纳米结构,金属电极的记录阻抗可以得到降低,并且神经刺激的电荷注入上限可以得到提升49,而这些表面微纳结构可以通过导电聚合物等材料修饰而实现。例如电化学修饰的PEDOT (Poly(3,4-ethylenedioxythiophene))碳纳米管50或PEDOT离子液体51可以有效地降低电极表面的阻抗且其表面均有丰富的纳米结构,从而提高电极信噪比。另一方面,神经电极也可以通过导电聚合物材料修饰实现高时空精度的精准药物控制释放52或者神经递质和其他神经活性分子例如可卡因53的检测功能,从而进一步拓展脑机接口与其周围神经元之间的信息沟通能力。另一种可能的调控方式是采用复合了光电极和液体通道(如图2F,2I)54或增加微流控通道从而使用药物调控(如图2D)55,但该类器件制备相对复杂。相比之下,传统电极仅能进行电信号的采集,并通过电刺激对周围神经元进行一定的兴奋或抑制的无差别刺激,而无法精确调控特定神经递质受体的活动。
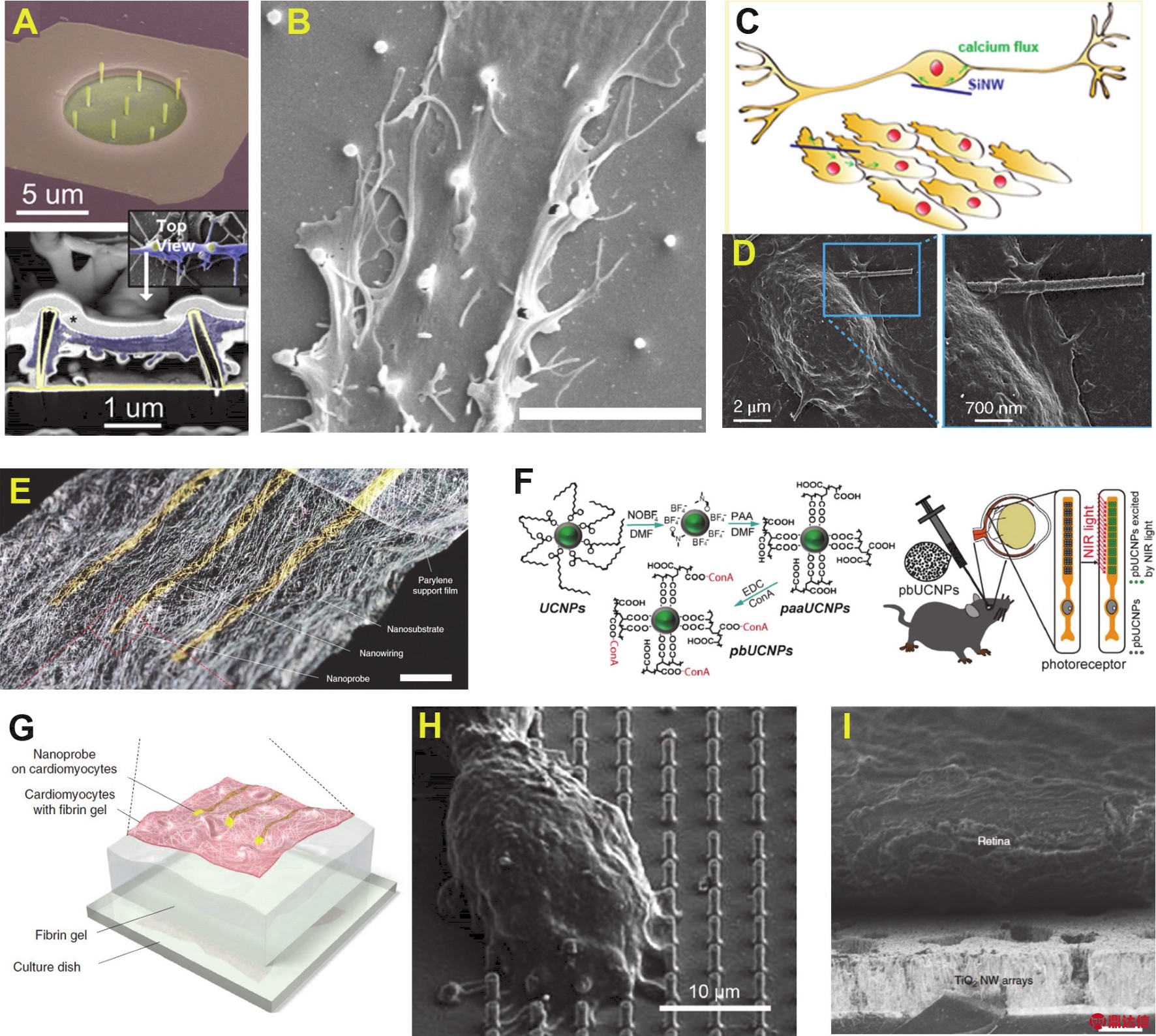
图3 神经记录与刺激的界面纳米材料与应用
Fig.3 Application of nanomaterial and nanodevices in neural recording and stimulation.
(A)Membrane electrode with nanopillars 72; (B)SEM of nanopillar device 91; (C)Optical modulation of cellular activity with SiNW (silicon nanowire)74;(D)Optical modulation of neurons with silicon nanowire 75; (E)SEM of ultrasoft nanowire electrodes 49a; (F)Nanoparticle to enable infrared vision in mice (UCNP,Upconversion Nanoparticles)80; (G)Interface of ultrasoft electrode with cardiomyocytes 49a; (H)Subcellular interface nanopillar device 85; (I)Nanowire arrays to restore vision in blind mice 80.(A,C,H)Reprinted with permission from American Chemical Society.(B,D,(E),G,I)Reprinted with permission from Springer Nature.(F)Reprinted with permission from Elsevier.
3.2 在体神经界面纳米材料与器件的发展
鉴于半导体纳米器件的加工精度、生物相容性和灵活的物理性质,这些器件可能用于开发下一代神经界面56。由于纳米场效应管尺寸可以加工到10 nm甚至更小,并且其记录性能不受电极阻抗影响,因此在微纳神经器件方向具有很大的潜力57。由于神经信号调控或消耗纳米场效应管沟道中的电子能力远强于对大尺寸场效应管的调控,因此这些器件能提供极好的电压敏感性58。并且由于场效应管的内源延迟时间与尺寸系数L成反比,因此这些器件可以达到极高采集速度。过去十年产生了众多新兴的纳米场效应管构型,包括弯折纳米线59,弯曲纳米线60,硅纳米线合并氧化物纳米管支链57,61,硅纳米管62,超短通道蚀刻纳米线24a,纳米薄膜63,多孔微粒64,石墨烯65等,当然也有整合成网状结构的纳米电子元件23a,32a,66。另一方面,半导体聚合物的纳米约束也已实现了拉伸性好,体积小的晶体管67。上述很多种纳米场效应管都可以用于记录膜电位或胞外场电位信号,并且不同的场效应管还可能实现慢性38b,68或急性63,69不同场景的应用。此外,柔性SU-8基底上的弯折纳米线场效应管也可以构成三维电极阵列从而采集细胞膜电位59,并且磷脂分子镀层修饰的场效应管还可以实现仿细胞膜的性质,从而改善其插入细胞膜内或跨膜记录的能力。另外,可响应的分子驱动器还可以让细胞膜局部稳定性降低,从而辅助采集元件的侵入记录70,这些驱动器通常可以用可见光、近红外、紫外或射频信号所激发71。
某些纳米材料在生物电信号记录和电刺激等方面的应用已经产生了一些重要进展,例如通过近红外激光辐照,金纳米管可以实现细胞膜局部穿孔,从而实现细胞膜内与膜外电位的同时采集(如图3A)72;进一步使用此原理,多孔纳米铂薄膜可通过光声穿孔的原理实现超灵敏电信号采集或刺激73;通过硅纳米线或阵列结构的光热效应可以用于调控心肌细胞(如图3C)74或者神经元(如图3D)75的活动;微纳尺寸的蘑菇状金属电极可以通过细胞内吞作用而实现跨膜记录胞内电位的效果76,通过类似原理,垂直的纳米柱77,纳米管78和有金属镀层的半导体纳米线79也被证明可以用于胞内记录或刺激。另一项研究中心,柔性纳米线网可以记录心肌细胞的活动49a (如图3E,G)光激活纳米颗粒或纳米线也可以刺激视网膜实现视觉的替代或增强(如图3F,I)80。在无线记录或刺激系统的开发方面,目前已经涌现大量相关的技术。例如MoS2二维材料可能作为Wi-Fi频段能量传输的器件(如图4A)81;采用超声器件已经可以实现外周神经的无线记录82 (如图4B,D);通过合成模拟细胞膜和离子通道特性的纳米场效应管器件可以实现光控的膜电位变化(如图4C)83;通过无线可降解的电极等可以实现持续可控的神经再生治疗过程(如图4E)69;而利用细胞级尺寸的微型光电元器件也已经可以实现无线光遗传(如图4F,G)84。这些方法的出现可能给无线神经刺激或记录界面技术的发展带来一系列重要突破。
而另一方面,纳米材料和纳米结构在组织界面的生物过程研究方面也已经显示了一些优势,例如Santoro等85研究发现纳米结构的细节对细胞贴附、慢性炎症反应等都可能起到重要的调控作用(如图3H)。另一项研究中,同时,在柔性和多孔聚合物基底上面加工纳米尺度电极32a,66,68可以实现机械性能较好的二维或三维电极阵列。除了网状电极外,使用聚合物基底上的铂或者金电极,已经可以实现迄今尺寸最小的神经电极——纳米丝线86。另外,目前的电极加工技术还可以将电极整合到其他器件平台基础上,例如微流控通道壁上面整合的微电极可以做在体神经肌肉接头的信号研究87。
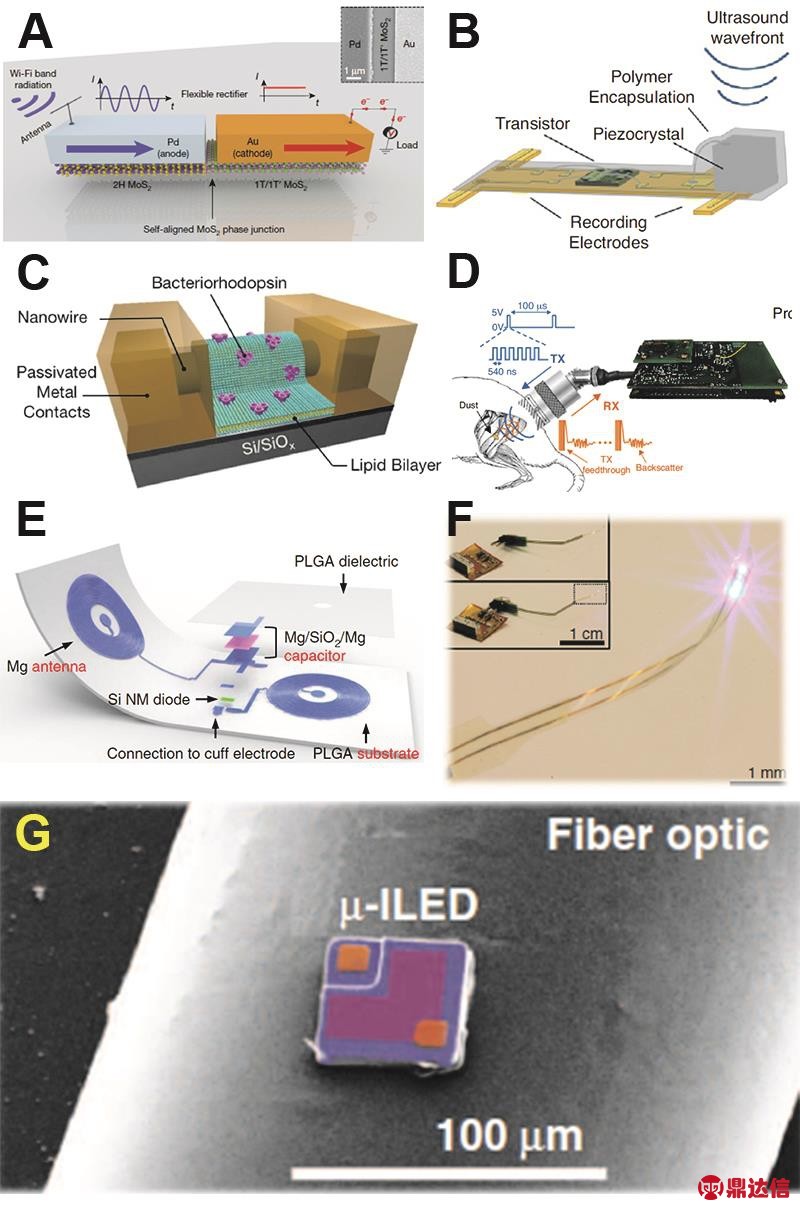
图4 用于无线神经界面的纳米神经元器件
Fig.4 Wireless neural interface devices.
(A)Nano-transistor device for wireless energy harvest 81; (B)Neural dust wireless device 82; (C)FET (Field Effect Transistor)device with Bacteriorhodopsin 83; (D)Neural dust device system 82; (E)Fully resorbable stimulation device 69; (F)Optogenetics device 84; (G)SEM of wireless optogenetics device (μ-ILEDs microscale,Inorganic Light-Emitting Diodes)84.(A,E)Reprinted with permission from Springer Nature.(B,D)Reprinted with permission from Elsevier.(C)Reprinted with permission from John Wiley and Sons.(F,G)Reprinted with permission from The American Association for the Advancement of Science.
同时,一些纳米颗粒类的材料也有潜力成为无线记录神经活动乃至细胞器活动的元器件。静息状态下,神经元膜电位为-70 mV左右,当有兴奋性输入时,可能会产生几毫伏的阈下波动或者120 mV左右的动作电位。但该电位在细胞膜上面能产生的电场强度由于膜厚度可以变得非常强,因此,电场强度响应的纳米元件,例如量子点,可能用于读取膜电位88。当电场变化时,量子点的发光波长迅速红移并且光强减弱89。但目前仅60 nm以下尺寸的量子点可能被装到类细胞膜的载体上90,而大多数量子点很难被整合到神经元的膜上,这一定程度限制了这些材料的应用。与细胞器尺寸在同一级别的纳米结构可能具备低细胞毒性的特征,并且可以通过多种途径被转运到胞内工作(如图3B)91。例如,纳米级荧光钻石颗粒92和内吞金纳米杆93等可以定位到胞内体上,并可以对轴突转运进行实时监测92。另外,内质网和线粒体等细胞器也可以被具有光热效应的金纳米颗粒94或纳米硅器件(如图3C)75,95所调控,从而调节胞内的钙离子浓度和代谢水平。但是在使用光热效应激活纳米器件的过程中,需要考虑可能同时带来的活性氧自由基或其他可能产生细胞毒性的效应要尽可能避免96。另一类纳米器件,DNA (脱氧核糖核酸)纳米笼,可以用作向胞内局部转运生物活性分子97或者生物传感器分子,例如钙离子98、氯离子99或pH值99c的指示剂,从而加深对胞内离子浓度调控神经活动机制的理解。针对这些纳米器件的进一步开发和应用可能成为下一代无线神经记录与调控的重要方式。
4 总结与展望
以上谈及的神经电极器件与材料都属于神经界面研究领域。神经界面是一个新兴的研究领域,它是随着神经工程和脑机接口技术的兴起而发展起来的。目前在神经界面的材料与器件领域已经涌现出大量的前沿进展,包括Neuropixel等微纳加工的电极阵列技术和场效应管等纳米级神经调控和记录器件和硅纳米线等材料,这些新技术已经针对性地在神经界面性能方面实现了一系列的提升,包括:透明度,柔软性,拉伸性,良品率,工艺精度,信号长期稳定性,能否无线传输,单位体积内通道数,能否贴附或穿过细胞膜等等。并且一些种类材料与器件的工程就绪度已经十分接近成功商业转化所需的要求。
从脑神经的角度,大脑需要一条与外部世界直接交互的途径,而不是仅仅依赖于天然的五官以及手脚。无论是治疗脑神经疾病、提供脑控机械肢体还是研究脑神经功能的基础神经科学研究,都需要一个外部媒介来把脑神经信息提取并转发到外部的电子计算机信息世界中,同样也要把外部计算机信息传递给脑神经。而这个脑机媒介物,是个外来物,它怎么融合到脑组织中与神经系统和睦的无障碍沟通信息就是神经界面的研究目的和内容。在介观尺度上,它负责准确地获取脑内一定范围内神经网络的活动规律;在微观尺度上,它需要和特定功能的神经元近距离沟通代表神经信息的电信号;在纳观尺度上,它还要在拥挤的胞外基质中与各种神经递质、细胞受体,胞外大分子蛋白进行密切的物质与能量交换。神经界面研究可以说是神经科学、生物技术、微纳加工、纳米技术与材料科学的结合与综合研究。而神经电极作为这个媒介物的一种主要形式,它的理想设计与实现的发展方向是要同时涵盖介观、微观以及纳观层面上与神经结构交互的要求。